(München) – Sowohl Brennstoffzellen, die Wasserstoff in Strom umwandeln, als auch Elektrolyseure, die durch Wasserspaltung mithilfe von Strom Wasserstoff herstellen, brauchen als Katalysator das Edelmetall Platin. Es ist selten und teuer. Allerdings katalysieren auch Enzyme, sogenannte Hydrogenasen, die Umwandlung von Wasserstoff „sehr schnell und nahezu ohne Energieverlust“, erklären Wissenschaftler der Technischen Universität München (TUM). Jedoch galten diese Biokatalysatoren bisher als „ungeeignet für den industriellen Einsatz, da sie hoch empfindlich gegen Sauerstoff sind“.
Einem Forschungsteam ist es laut TUM gelungen, „die empfindlichen Enzyme so in ein schützendes Polymer einzubauen, dass sie auch für die technische Wasserstoffumwandlung eingesetzt werden können“. Daran beteiligt sind die TU München, die Ruhr-Universität Bochum, das CNRS Marseille und das Max-Planck-Instituts für Chemische Energiekonversion in Mülheim an der Ruhr (CEC)
Wenig Schaden durch Sauerstoff
„Bettet man die empfindlichen Hydrogenasen in geeignete Polymere ein, so arbeiten sie auch in Gegenwart von Sauerstoff mehrere Wochen“, sagt Nicolas Plumeré, Professor für Elektrobiotechnologie am TUM Campus Straubing für Biotechnologie und Nachhaltigkeit. „Ohne diesen Schutz verlieren sie ihre Aktivität innerhalb von Minuten.“
Das Einbetten in sogenannte Redox-Polymere, Kunststoffe, deren Seitengruppen Elektronen übertragen können, hatte bisher einen entscheidenden Nachteil, so die Forscher: „Sie setzten dem Fluss von Elektronen einen hohen Widerstand entgegen.“ Um diesen zu überwinden, habe man „Energie investieren“ müssen. Aufgrund der dabei entstehenden Wärme hätten die Hydrogenasen die Fähigkeit, Wasserstoff zu erzeugen, eingebüßt. Durch Feinabstimmungen in der Polymermatrix haben die Wissenschaftler erreicht, dass die Hydrogenase die Reaktion ohne Energieverlust in beiden Richtungen katalysieren.
Effizienz nahe 100 Prozent
Mit diesem System baute das Forschungsteam eine Brennstoffzelle auf. Dabei wird durch ein Bakterium (Myrothecium verrucaria) der Sauerstoff reduziert, ein weiteres Bakterium (Desulfovibrio desulfuricans) oxidiert den Wasserstoff und erzeugt Strom. Auch für die umgekehrte Reaktion, die Wasserstoffproduktion durch Aufnahme von Elektronen, sei das System einsetzbar: „Seine Effizienz bei der Energieumwandlung liegt auch bei Stromdichten von über vier Milliampere pro Quadratzentimeter nahe 100 Prozent“, so die Wissenschaftler.
Die Verringerung des Energieverlusts habe zwei Vorteile, sagt Nicolas Plumeré: „Das System wird dadurch nicht nur wesentlich effizienter. Bei hohen Leistungen wäre die in einem Brennstoffzellen-Stack entstehende Wärme für die biologischen Systeme ein Problem.“ Die weitere Forschung des Teams zielt nun drauf ab, die Stabilität der Hydrogenasen bei höheren Stromdichten zu verbessern, um Systemen mit Katalysatoren auf Platin-Basis Konkurrenz machen zu können.
Die Forschungsarbeiten wurden gefördert durch das European Research Councils (ERC), das französische Centre Nationale de la Recherche Scientifique (CNRS) und die Aix-Marseille Université, die Deutsche Forschungsgemeinschaft (DFG) im Rahmen einer Gemeinschaftsförderung zusammen mit der Agence Nationale de la Recherche, die Max-Planck-Gesellschaft sowie durch das Bundesministerium für Bildung und Forschung (BMBF).
Deep Link
https://idw-online.de/de/news768692
Publikation
„Reversible H2 oxidation and evolution by hydrogenase embedded in a redox polymer film“. Steffen Hardt, Stefanie Stapf, Dawit T. Filmon, James A. Birrell, Olaf Rüdiger, Vincent Fourmond, Christophe Léger, Nicolas Plumeré. Nature Catalysis Vol. 4, 251–258 (2021) – DOI: 10.1038/s41929-021-00586-1
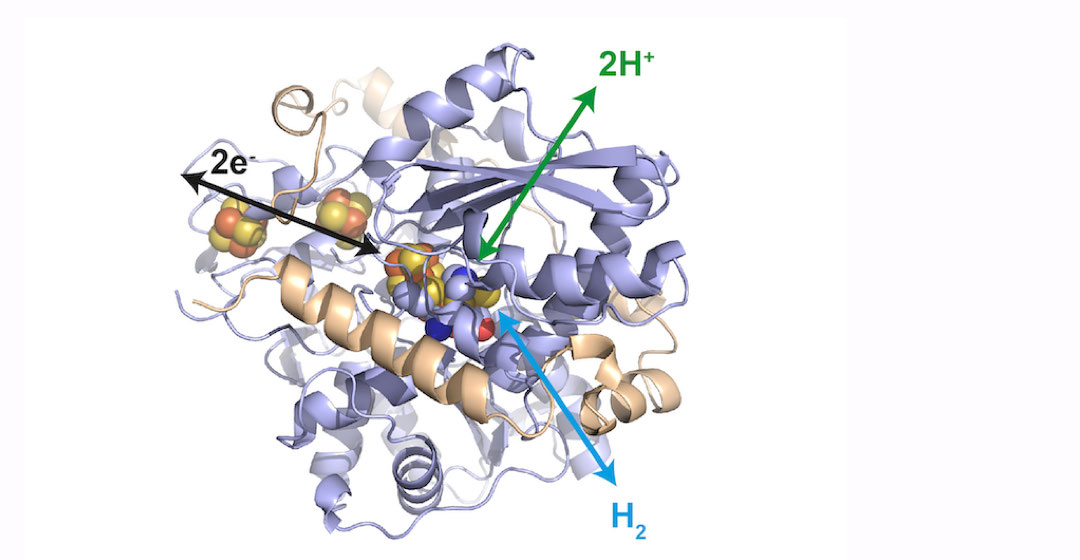
Illustration
Ein Eisen-Schwefel-Cluster im Inneren der Hydrogenase katalysiert die Oxidation des Wasserstoffs zu Protonen beziehungsweise die Reduktion von Protonen zu Wasserstoff. Weitere Eisen-Schwefel-Cluster ermöglichen die Weiterleitung der Elektronen. / © James Birrell / MPI CEC